《2022年高中化學(xué) 每日一題之快樂暑假 第08天 原電池(含解析)新人教版》由會(huì)員分享�,可在線閱讀,更多相關(guān)《2022年高中化學(xué) 每日一題之快樂暑假 第08天 原電池(含解析)新人教版(4頁珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索���。
1��、2022年高中化學(xué) 每日一題之快樂暑假 第08天 原電池(含解析)新人教版
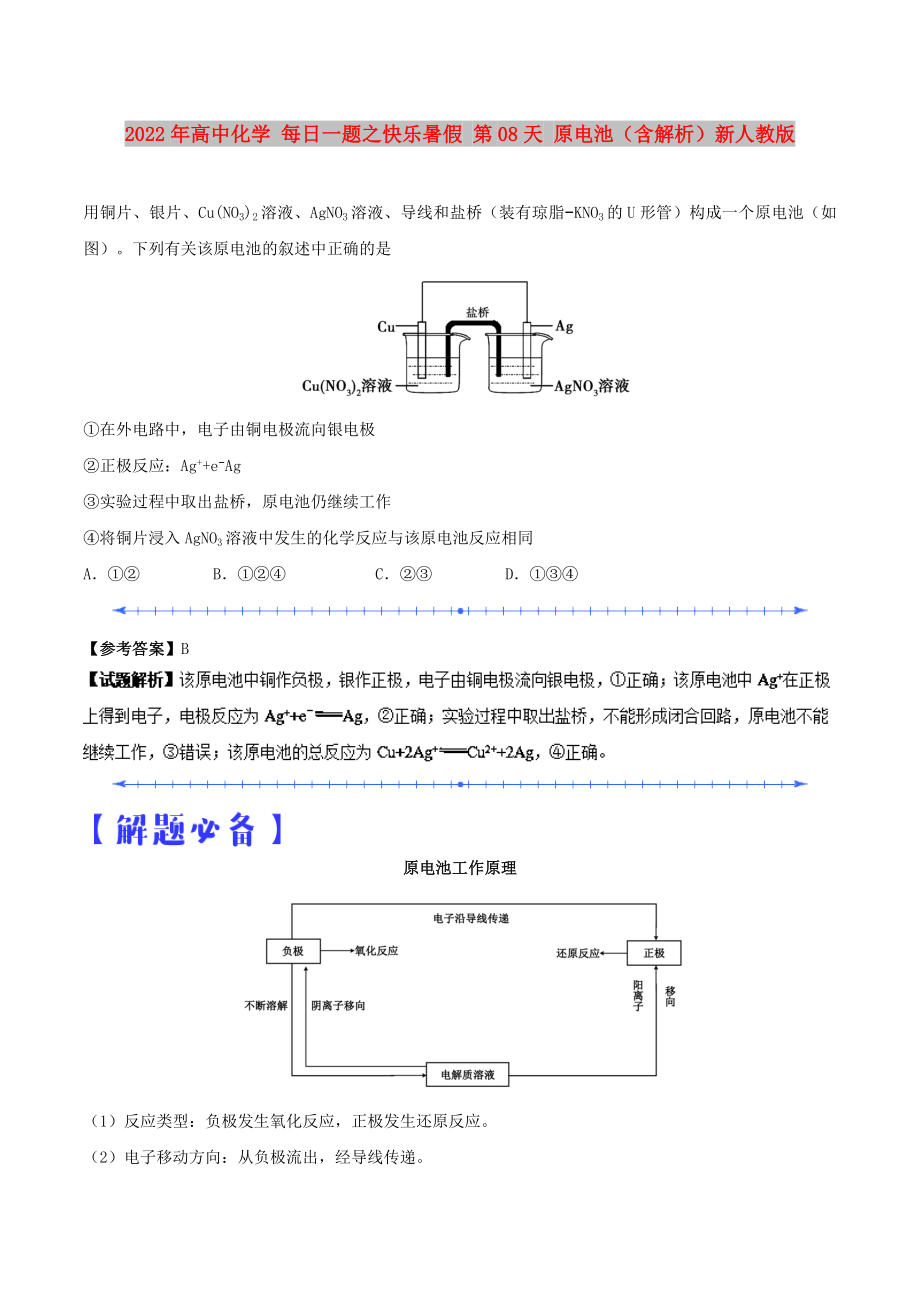
用銅片��、銀片���、Cu(NO3)2溶液����、AgNO3溶液���、導(dǎo)線和鹽橋(裝有瓊脂?KNO3的U形管)構(gòu)成一個(gè)原電池(如圖)����。下列有關(guān)該原電池的敘述中正確的是
①在外電路中���,電子由銅電極流向銀電極
②正極反應(yīng):Ag++e?Ag
③實(shí)驗(yàn)過程中取出鹽橋�,原電池仍繼續(xù)工作
④將銅片浸入AgNO3溶液中發(fā)生的化學(xué)反應(yīng)與該原電池反應(yīng)相同
A.①② B.①②④ C.②③ D.①③④
【參考答案】B
原電池工作原理
(1)反應(yīng)類型:負(fù)極發(fā)生氧化反應(yīng)��,正極發(fā)生還原反應(yīng)��。
(2)電子移動(dòng)方
2��、向:從負(fù)極流出���,經(jīng)導(dǎo)線傳遞����。
(3)離子的移動(dòng)方向:陽離子向正極移動(dòng)���,陰離子向負(fù)極移動(dòng)�。
1.下列說法正確的是
A.原電池中,負(fù)極上發(fā)生的反應(yīng)是還原反應(yīng)
B.原電池中�,電流的方向是負(fù)極?導(dǎo)線?正極
C.雙液原電池中的鹽橋是為了連通電路,所以也可以用金屬導(dǎo)線代替
D.在原電池中����,陽離子移向正極���,陰離子移向負(fù)極
2.在理論上不能用于設(shè)計(jì)原電池的化學(xué)反應(yīng)是
A.H2SO4(aq)+BaCl2(aq)2HCl(aq)+BaSO4(s) ΔH<0
B.2CH3OH(l)+3O2(g)2CO2(g)+4H2O(l) ΔH<0
C.4Fe(OH)2(s)+2H2O(l)+O2(g)4
3����、Fe(OH)3(s) ΔH<0
D.3Cu(s)+8HNO3(aq)3Cu(NO3)2(aq)+2NO(g)+4H2O(l) ΔH<0
3.原電池的正極一定是
A.化學(xué)性質(zhì)較活潑的金屬 B.化學(xué)性質(zhì)較不活潑的金屬
C.電子流出的一極 D.電子流入的一極
4.有甲���、乙兩個(gè)裝置����,下列說法錯(cuò)誤的是
甲 ????? ????? 乙
A.甲�、乙裝置中,Zn的質(zhì)量均減小
B.甲����、乙裝置中��,Cu上均有氣泡產(chǎn)生
C.化學(xué)反應(yīng)速率:乙>甲
D.甲裝置中H+移向Zn����,乙裝置中H+移向Cu
5.將NaCl溶液滴在一塊光亮清潔的鐵板表面
4����、上,一段時(shí)間后發(fā)現(xiàn)液滴覆蓋的圓周中心區(qū)(a)已被腐蝕而變暗����,在液滴外沿形成棕色鐵銹環(huán)(b),如圖所示�。導(dǎo)致該現(xiàn)象的主要原因是液滴之下氧氣的含量比邊緣的少。下列說法正確的是
A.液滴下氧氣的含量少�,發(fā)生析氫腐蝕
B.液滴下的Fe因發(fā)生還原反應(yīng)而被腐蝕,生成的Fe2+由(a)區(qū)向(b)區(qū)遷移���,與(b)區(qū)的OH?形成Fe(OH)2����,進(jìn)一步被氧化��、脫水形成鐵銹
C.液滴邊緣是正極區(qū)���,發(fā)生的電極反應(yīng)為O2+2H2O+4e?4OH?
D.若改用嵌有一銅螺絲釘?shù)蔫F板����,在銅鐵接觸處滴加NaCl溶液,則負(fù)極發(fā)生的電極反應(yīng)為Cu-2e?Cu2+
6.甲中盛有0.1 mol/L稀硫酸�,乙中盛有0.1
5、mol/L CuCl2溶液(兩種溶液均足量)�,裝置如圖所示,下列說法不正確的是
A.甲為原電池��,乙為電解池
B.甲裝置給乙裝置提供電能
C.當(dāng)甲中產(chǎn)生0.1 mol氣體時(shí)��,乙中產(chǎn)生氣體的物質(zhì)的量也為0.1 mol
D.一段時(shí)間后�����,甲中溶液的pH增大
1.【答案】D
【解析】A項(xiàng)��,負(fù)極上發(fā)生氧化反應(yīng)���。B項(xiàng),電流的方向應(yīng)是正極?導(dǎo)線?負(fù)極��。C項(xiàng)�����,鹽橋不能用導(dǎo)線代替。
2.【答案】A
3.【答案】D
【解析】原電池的正極材料可以是金屬�、非金屬或金屬氧化物等,但無論是哪種材料�,正極上都發(fā)生還原反應(yīng),是電子流入的一極�����。
4.【答案】B
5.【答案】C
【解析】液滴邊
6�����、緣O2較多�,在微弱的酸性或中性條件下易發(fā)生吸氧腐蝕,鐵板中碳粒上發(fā)生的正極反應(yīng)為O2+2H2O+4e?4OH?���,A錯(cuò)誤�;液滴下的Fe失去電子��,發(fā)生氧化反應(yīng)而被腐蝕���,負(fù)極反應(yīng)式為Fe?2e?Fe2+�����,為腐蝕區(qū)(a)��,B錯(cuò)誤�;液滴邊緣氧氣多,O2得電子被還原���,C項(xiàng)正確�����;Cu比Fe更穩(wěn)定�����,F(xiàn)e作負(fù)極,Cu作正極�,負(fù)極反應(yīng)式為Fe?2e?Fe2+,D項(xiàng)錯(cuò)誤���。
6.【答案】B
【解析】構(gòu)成甲裝置的是活動(dòng)性不同的兩個(gè)電極��、電解質(zhì)溶液且兩極形成了閉合回路�,顯然甲裝置為原電池,且甲為乙的電解提供電能�。電極反應(yīng)分別如下:甲中2H++2e?H2↑(正極),F(xiàn)e?2e?Fe2+(負(fù)極)��;乙中Cu2++2e?Cu(陰極)�����,2Cl??2e?Cl2↑(陽極)�,綜上,B錯(cuò)誤�����。
你正走在學(xué)霸的路上��!
_____________________________________________________________________________
_____________________________________________________________________________
 2022年高中化學(xué) 每日一題之快樂暑假 第08天 原電池(含解析)新人教版
2022年高中化學(xué) 每日一題之快樂暑假 第08天 原電池(含解析)新人教版