《北京市延慶縣靳家堡中學(xué)九年級(jí)化學(xué)下冊(cè) 課堂檢測(cè)(酸堿鹽反饋)2(無(wú)答案) 人教新課標(biāo)版(通用)》由會(huì)員分享��,可在線(xiàn)閱讀����,更多相關(guān)《北京市延慶縣靳家堡中學(xué)九年級(jí)化學(xué)下冊(cè) 課堂檢測(cè)(酸堿鹽反饋)2(無(wú)答案) 人教新課標(biāo)版(通用)(2頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索��。
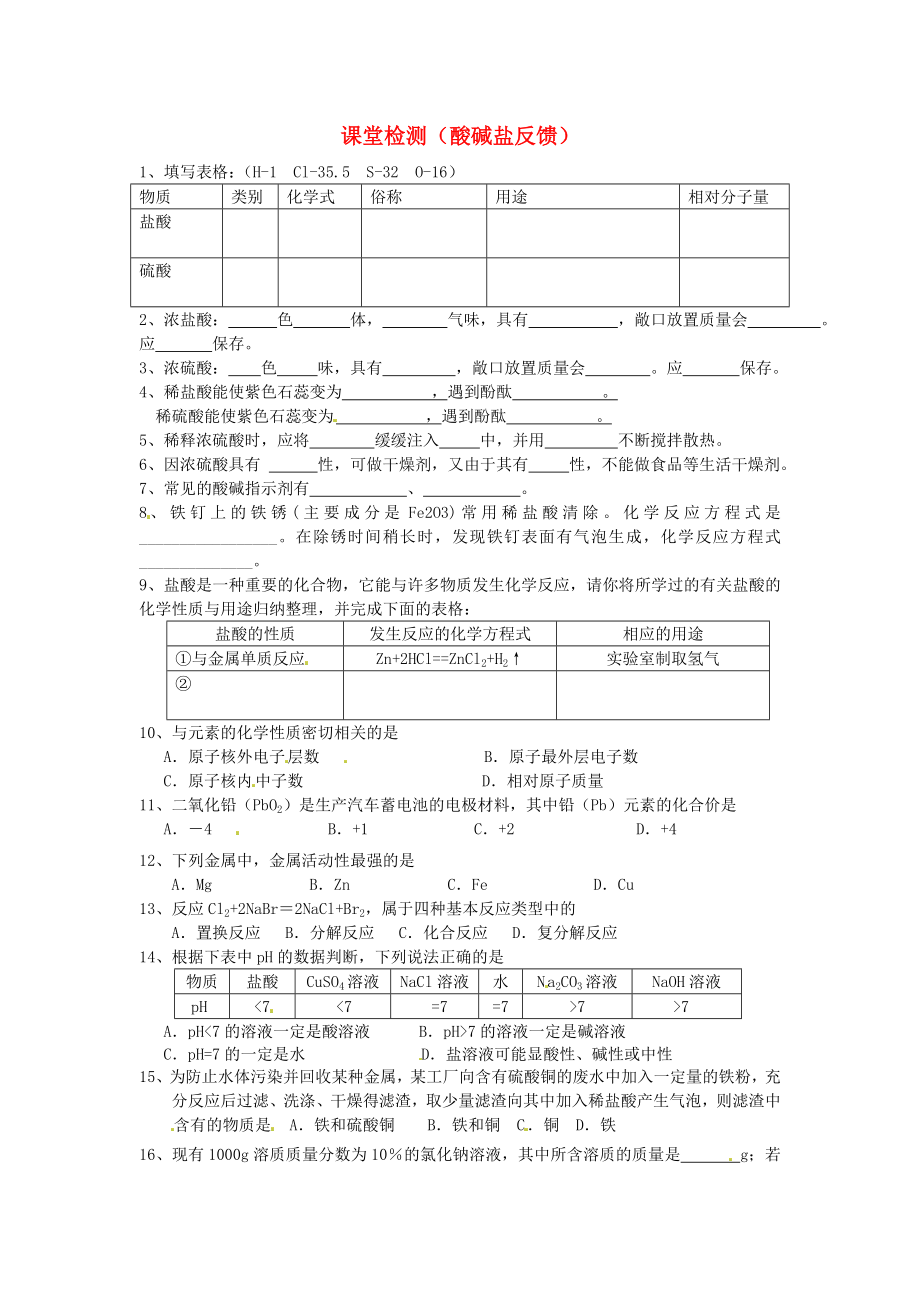
1�、課堂檢測(cè)(酸堿鹽反饋)
1��、填寫(xiě)表格:(H-1 Cl-35.5 S-32 O-16)
物質(zhì)
類(lèi)別
化學(xué)式
俗稱(chēng)
用途
相對(duì)分子量
鹽酸
硫酸
2����、濃鹽酸: 色 體, 氣味�,具有 ,敞口放置質(zhì)量會(huì) �����。應(yīng) 保存���。
3�、濃硫酸: 色 味���,具有 �����,敞口放置質(zhì)量會(huì) �。應(yīng) 保存�����。
4���、稀鹽酸能使紫色石蕊變?yōu)? �,遇到酚酞 �����。
稀硫酸能使紫色石蕊變?yōu)?
2���、 �����,遇到酚酞 ��。
5����、稀釋濃硫酸時(shí),應(yīng)將 緩緩注入 中����,并用 不斷攪拌散熱。
6����、因濃硫酸具有 性,可做干燥劑��,又由于其有 性�,不能做食品等生活干燥劑。
7�、常見(jiàn)的酸堿指示劑有 、 ��。
8�����、鐵釘上的鐵銹(主要成分是Fe2O3)常用稀鹽酸清除���?����;瘜W(xué)反應(yīng)方程式是_________________�����。在除銹時(shí)間稍長(zhǎng)時(shí)���,發(fā)現(xiàn)鐵釘表面有氣泡生成,化學(xué)反應(yīng)方程式______________�����。
9����、鹽酸是一種重要的化合物,它能與許多物質(zhì)發(fā)生化學(xué)反應(yīng)�����,請(qǐng)你將所學(xué)過(guò)的
3��、有關(guān)鹽酸的化學(xué)性質(zhì)與用途歸納整理����,并完成下面的表格:
鹽酸的性質(zhì)
發(fā)生反應(yīng)的化學(xué)方程式
相應(yīng)的用途
①與金屬單質(zhì)反應(yīng)
Zn+2HCl==ZnCl2+H2↑
實(shí)驗(yàn)室制取氫氣
②
10�����、與元素的化學(xué)性質(zhì)密切相關(guān)的是
A.原子核外電子層數(shù) B.原子最外層電子數(shù)
C.原子核內(nèi)中子數(shù) D.相對(duì)原子質(zhì)量
11��、二氧化鉛(PbO2)是生產(chǎn)汽車(chē)蓄電池的電極材料���,其中鉛(Pb)元素的化合價(jià)是
A.-4 B.+1 C.+2
4、 D.+4
12��、下列金屬中�����,金屬活動(dòng)性最強(qiáng)的是
A.Mg B.Zn C.Fe D.Cu
13���、反應(yīng)Cl2+2NaBr=2NaCl+Br2���,屬于四種基本反應(yīng)類(lèi)型中的
A.置換反應(yīng) B.分解反應(yīng) C.化合反應(yīng) D.復(fù)分解反應(yīng)
14、根據(jù)下表中pH的數(shù)據(jù)判斷�����,下列說(shuō)法正確的是
物質(zhì)
鹽酸
CuSO4溶液
NaCl溶液
水
Na2CO�3溶液
NaOH溶液
pH
<7
<7
=7
=7
>7
>7
A.pH<7的溶液一定是酸溶液 B.pH>7的溶
5、液一定是堿溶液
C.pH=7的一定是水 D.鹽溶液可能顯酸性���、堿性或中性
15��、為防止水體污染并回收某種金屬�,某工廠(chǎng)向含有硫酸銅的廢水中加入一定量的鐵粉����,充分反應(yīng)后過(guò)濾���、洗滌�、干燥得濾渣���,取少量濾渣向其中加入稀鹽酸產(chǎn)生氣泡�,則濾渣中含有的物質(zhì)是 A.鐵和硫酸銅 B.鐵和銅 C.銅 D.鐵
16����、現(xiàn)有1000g溶質(zhì)質(zhì)量分?jǐn)?shù)為10%的氯化鈉溶液,其中所含溶質(zhì)的質(zhì)量是 g���;若將此溶液稀釋為4%的稀溶液���,需加水 g��。
 北京市延慶縣靳家堡中學(xué)九年級(jí)化學(xué)下冊(cè) 課堂檢測(cè)(酸堿鹽反饋)2(無(wú)答案) 人教新課標(biāo)版(通用)
北京市延慶縣靳家堡中學(xué)九年級(jí)化學(xué)下冊(cè) 課堂檢測(cè)(酸堿鹽反饋)2(無(wú)答案) 人教新課標(biāo)版(通用)